|
理化教師在國中所擔任的課程包括物理與化學,而物理與化學均屬於物質科學的一門探究物質的實驗科學。理化實驗常使用具體的實物,在適當控制的條件下可以實際操作,以產生可測量或觀察的現象,利用實際的感官以形成知識概念,因此實驗在中等教育顯得格外重要。不過日前實驗在中等學校實施的情形很不理想。實驗的器材雖然是一個問題,但是課程的繁重以及升學考試的壓力,實在是實驗實施不良的主要原因。要紓解教學的時間壓力以及學生的課業負擔,比較節省時間而又能讓學生親眼目睹物理現象以及化學變化,以助學生了解物理或化學原理,並提高學生學習理化的興趣,最好的方法就是教師在課堂上配合教學內容的演示實驗。
近年來,在國外的化學教育刊物上,出現Demistry與Chemdems等新名詞,前者是「化學」Chemistry的前四個字母Chem用「演示」Demonstration的前三個字母Dem所取代者,意即Demonstration for Chemistry Experiments。至於Chemdems是由化學與演示的兩個英文字的前幾個字母複合而成,可以解釋為 Demonstration that bring Chemistry to life.由此可見演示實驗在化學的重要性了。因為在課常上演示化學實驗,可使學生貫注精神,以觀察化學現象(變化)。配合課程的理化教師的演示實驗便於教師講解,易於學生了解物理與化學的原理,更可使學生留下深刻的印象,從而提高其學習理化的興趣。
許多教師認為教學是藝術與技術。藝術重視創新,技術講究方法。因此教學方法的創新與改進是理化教育的一個重要課題。優良的教學方法可使學生的學習事半功倍。教育心理學常說學童對於喜歡的事,容易做得好,因此喜歡與興趣可說是學生學好理化的原動力。簡單而有趣的實驗,有助於學生的學習。本刊這一期以「趣味科學實驗」為名,介紹一些PAC(Plain and Attractive Chemistry)簡而有趣的化學實驗,與PAP(Plain and Attractive Physics)簡而有趣的物理實驗,與理化教師共勉,敬請參酌指正。
|
| 可燃的鐵 |
| 一、目的 |
加熱分解草酸鐵,以製備微細的鐵粉。比較鐵釘、鋼絲絨、與鐵粉的可燃性,進而探討微細鐵粉的自燃。
|
| 二、器材 |
草酸鐵 2克
蠟燭 1支
酒精燈 1個
打火機 1個
試管與橡皮塞 1組
鐵釘 1支
試管夾(鐵製) 1支
鑷子 1支
試管架 1個
鋼絲絨 1塊
磁鐵 1個
鋁箔(約30X40cm2) 1張
玻棒 1支
面紙 1張
|
| 三、實驗步驟 |
| (一)微細鐵粉的製備 |
1.用試管取黃色的草酸鐵(FeC2O4‧2H2O)約 2 克。
2.用試管夾(鐵製)夾住試管,用酒精燈的火焰加熱。注意要先加熱試管的上端,然後加熱試管底部的草酸鐵,並用玻棒攪拌草酸鐵(如圖一),使其受熱均勻。
|
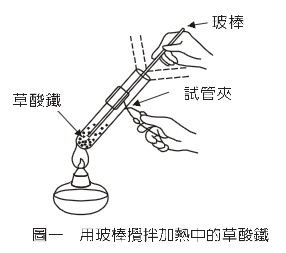
圖一 用玻棒攪拌加熱中的草酸鐵 |
|
3.黃色的草酸鐵受熱分解 • 逐漸變成灰色粉末而浮動。繼續加熱並攪拌至粉末不再浮動,而且變成黑色。
4.試管移開火焰後,放置於試管架上,立即蓋上橡皮擦(先輕輕地蓋)
5.稍冷(用手可以觸摸的程度)後蓋緊橡皮塞。然後點燃一支蠟燭,用其蠟汕密封試管口(如圖二)。 |
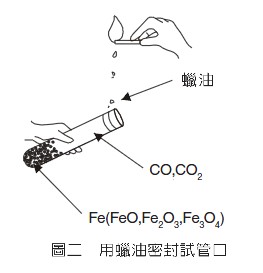
圖二 用蠟油密封試管口 |
|
【問1】寫出步驟3黃色草酸鐵受熱分解的反應式。
【問2】在步驟2,為什麼要先加熱試管的上端,然後才可加熱草酸鐵? |
| (二)鐵釘、鋼絲絨、與微細鐵粉的可燃性比較 |
1.先用磁鐵分別吸住鐵釘與鋼絲絨,然後用磁鐵從試管外而吸住微細的鐵粉末,上下移動磁鐵,可見鐵粉隨磁鐵上下移動。
2.鐵釘用鑷子夾住後移至酒精燈的火焰上,鐵釘並不會著火燃燒。
3.取鋼絲絨一小塊,先用手指將其鬆開後,用鑷子夾住,放在酒精燈的火焰上,即見鋼絲絨著火,發出火花(如圖三)。 |
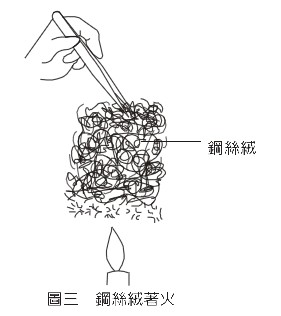
圖三 鋼絲絨著火 |
|
4.在地面上先舖一張鋁箔,並在鋁箔的中央部位放置一張面紙後,打開試管口的橡皮塞,略為傾斜地持試管(管口朝下,如圖四),用食指輕彈試管,使鐵粉紛紛落下,即見鐵粉離開試管,落地途中閃出小小火花(在暗處更明顯)。最後將較多的鐵粉,一起倒在面紙上,即見鐵粉點燃了面紙,使其燃燒起來(要注意火煙偵器)。
【問3】寫出鐵粉自燃發火的反應式。
|
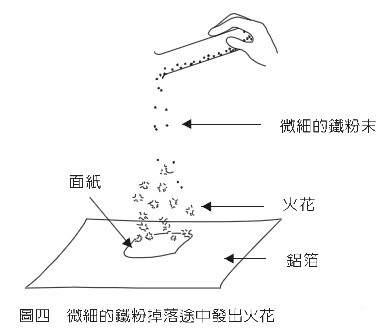
圖四 微細的鐵粉掉落途中發出火花 |
|
| 四、教師手冊 |
| (一)問題的參考答案 |
【問1】寫出步驟3黃色草酸鐵受熱分解的反應式:
|
|
【問2】在步驟2,為什麼要先加熱試管的上端,然後才可加熱草酸鐵?
避免草酸鐵受熱分解,由其所含的結晶水所產生的水蒸氣,如反應式(1)所示,在試管的上端凝結成水,倒流至試管受熱部分,導致試管破裂。
【問3】寫出鐵粉自燃發火的反應式。
|
|
| (二)補充說明 |
1.微細的鐵粉為什麼易燃?
(1)微細的粉木,表面積增大,與空氣接觸面增大,所以容易氧化而燃燒。但是若用機械的方式,任憑再怎麼磨細,也得不到本實驗所得那麼細微(幾近奈米級)的粉末,所以不會自燃。
(2)草酸鐵受熱分解產生微細的鐵粉末時,所加的能量也活化了粉末的表面。微細的鐵粉末如此活化了,而其表面積又增大,所以容易自燃。
2.為什麼當微細的鐵粉離開試管口,落地的途中會自燃?
鐵粉掉落時,與空氣摩擦所產生的一點熱,加上活化了的鐵粉與空氣一接觸,即被氧化時所產生的熱,導致鐵粉自燃。
3.在實驗步驟5,已密封了試管口的試管內微細鐵粉,必須用鋁箔包裹數層,以免萬一試管破裂,鐵粉一觸空氣即自燃,發生危險。經如此包裹保存的鐵粉,即使放置數月,也不會失去其自燃發火的性質。
4.本實驗的要訣在於步驟3,必須加熱至粉末不再浮動,而且變成黑色為止。這個加熱操作要小心,就不會有危險。
5.若在實驗步驟2,加熱一段時間,粉末有點變成灰色時,移開玻璃棒,並將試管口移近火焰,即見試管口會呈現淡藍色火焰,這是一氧化碳正在燃燒的現象。
6.約在1990年,筆者帶領學生做「鍊金師的夢」實驗,回收的鋅粉經沖洗數次後過濾,鋅粉放置於一個塑膠盤晾乾。盤上的鋅粉偶爾翻動,至乾後數日未經攪動,卻自行起火,塑膠盤著火冒煙燃燒。幸好筆者在場,發覺後立即處理,未成災,而得到難忘的教訓,說出親身的經驗與讀者分享。
7.本寶驗留下的鐵粉,必須妥善處理,且不可丟棄於字紙簍,以免發生災害。
|
| (三、參考資料)
|
1.日本化學會編,「對教師與學生有用的化學實驗」,東京化學同人p.61(1987)。
2.W.E.Kuhn, “Ultrafine Particles"p.225, Electrochemical Society, Inc., New York (1963)
|