
文/潘俊宏、林威佑、郭子安
圖/潘俊宏
.png) 前言
前言
氧化還原反應是化學中重要概念之一,所謂氧化還原反應是一種關於電子轉移的化學反應,而電解反應即為其中一種。在目前的中學課程中,電解硫酸銅溶液為介紹電解反應的實驗之一,除了實驗操作外,課程著重於電解產物種類的觀察,進而引進正負極的反應介紹,但對於產物(金屬銅) 的生長並無法藉課程所提供裝置對金屬生長過程進行觀察。
目前「十二年國民基本教育課程綱要總綱」(又稱 108 課綱) (1)中提出:教師在教學上應從激發學生對科學的好奇心為起始,引導學生主動探索與實驗操作,進而使學生能具備科學核心知識、探究實作與科學論證、溝通能力。在中學課程中,氧化還原的現象是可提供學生進行探究的主題之一,特別是在電解的部分,但局限於目前教材的實驗裝置,很難提供學生作進一步的現象探究,所以對電解實驗裝置便有改進需要了。在目前中學教材中,電解硫酸銅溶液實驗裡需要使用大量硫酸銅溶液,在實驗結束後廢液的處理便是一大問題,雖然目前各學校對廢液的處理有不同方法,但如何減少實驗中使用溶液的量便是重要課題。
本研究即是利用簡單的材料,設計一組可減少廢液量的微型裝置,提供給學生進行電解硫酸銅溶液的氧化還原實驗,經由此實驗裝置,學生在電解硫酸銅溶液時可觀察到金屬的金屬枝晶(metal dendrites)的生長情況,進而引導學生對金屬枝晶生長進行探究,重要的是在本實驗使用低濃度、低容量的裝置,以符合綠色化學之精神,更教導學生環保之概念。
.png) 壹、微型實驗裝置的材料與製作
壹、微型實驗裝置的材料與製作
本實驗裝置主要採用簡單、容易取得的材料(如: 壓克力板) 進行製作,當學生使用此微型裝置進行電解硫酸銅溶液實驗時,容易觀察實驗過程,以利學生進行學習、探究。
一、材料
壓克力板 (10 cm × 10 cm) 1片
壓克力黏著劑 1瓶
長尾夾 4個
銅線與銅片 適量
電池組 (數個串聯,或電源供應器) 1組
二、製作過程
Step 1 切割出適當大小的壓克力板(如圖1-1 ,板的尺寸可隨需求調整)。
Step 2 取其中一片壓克力板,用壓克力黏著劑塗於壓克力板四周,將切割出的小壓克力板黏於大壓克力板四周(如圖1-2)。
Step 3 取寬約3 ~5 mm 的銅片和適當長度的的銅線放入圖2中之壓克力板,並蓋上另一片壓克力板, 再加上四個長尾夾固定二塊壓克力板 (如圖2)。
Step 4 將壓克力板內加入電解液(如硫酸銅溶液)並接上電源 (如圖3), 便可進行電解實驗。

圖1-1. 切割出的壓克力板

圖1-2. 完成的反應裝置

圖2. 簡易電解反應實驗裝置

圖3. 簡易電解反應架構圖
.png) 貳、實驗操作
貳、實驗操作
實驗將以製作出的微型電解裝置來進行,實驗中使用電源供應器提供電壓以方便調整電壓大小(裝置如圖3),電解過程中使用手機或攝影機(高倍像素為佳) 拍攝與記錄銅金屬析出過程,以利實驗後的深入觀察、探究。
首先取0.001M硫酸銅溶液約2~5mL滴入微型電解裝置中,再調整銅片(正極) 和(負極) 的距離為1公分後,以電源供應器施加 15 V的直流電壓進行電解並以手機拍攝與記錄微型電解裝置中的反應過程,電解實驗銅金屬樹生長反應過程如表一所示。
電解進行時,發現在負極 (陰極) 銅線二側尖端處開始出現微小的團狀的金屬(如表一中5秒),隨電解的進行,負極尖端處生成樹狀銅金屬樹晶,金屬樹頂端開始向四周延伸(如表一中25秒),而經過一段時間後朝銅金屬樹晶向負極延伸速率加快(如表一中55秒和95秒),形狀漸成樹枝形。
當提高硫酸銅溶液濃度為0.006M時,維持正負極間的距離為 1 公分並施加 15 V 的直流電壓進行電解,以手機拍攝與記錄微型電解裝置中的反應過程,電解實驗銅金屬樹生長反應過程如表二所示。相同金屬從銅線尖端開始生成樹晶,再由樹晶頂端向四周生長,相較於電解0.001M硫酸銅溶液,開始生成時的樹晶較為茂密且整體形狀較近似為圓形(如表二中25秒),隨電解實驗的進行,樹晶偏向正極生長且形狀漸成橢圓形。
表1. 施加 15 V 的直流電壓進行電解 0.001M 硫酸銅溶液,銅金屬樹在不同時間的生長情況。
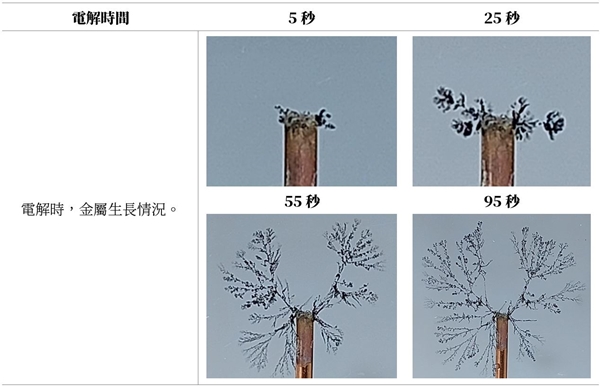 表2. 施加 15 V 的直流電壓進行電解 0.006M 硫酸銅溶液,銅金屬樹在不同時間的生長現象。
表2. 施加 15 V 的直流電壓進行電解 0.006M 硫酸銅溶液,銅金屬樹在不同時間的生長現象。

.png) 參、教學演示
參、教學演示
在目前的教材中,在電解實驗裡,學生使用U型管來進行電解硫酸銅溶液,實驗中只要求學生觀察正、負極產生物質的種類,而較難觀察到產物的生成樣貌。在使用微型電解裝置進行實驗時,可由直接觀察到銅金屬析出(如表1),教師可藉由此反應現象介紹發生電解的原理,開始進行電解時,為負極銅線尖端處開始出現的團狀的銅金屬,其主要原因為開始電解時,溶液中分布於銅線附近的銅離子由負極得到電子後,發生還原半反應後形成銅金屬沉積,逐漸形成了銅金屬樹晶,而在另一端的銅片(正極) 因失去電子形成銅離子溶於電解液中(實驗中較不易觀察),析出的銅離子和原電解液中的銅離子受到濃度差和電場作用也朝向負極移動,進而在銅金屬的樹晶尖端形成沉積,銅金屬越接近正極,使得銅金屬沉積越快,隨電解時間經過,便形成了銅金屬樹晶。若提高硫酸銅溶液的濃度且在施加相同電壓電解時,由於溶液中銅離子的濃度較高,銅金屬析出便較快、較密(比較表1和表2) 。
除了觀察到負極的產物(銅金屬) 外,學生亦可觀察到銅金屬樹晶析出的樣貌,可欣賞化學變化之美感,更可進一步觀察銅金屬樹晶析出的細部結構和外形,進行深入的科學探究;除此之外,亦可改變電解液中不同金屬種類和濃度,進行比較不同金屬樹晶析出、堆疊的樣貌與反應狀況,對各種變因進行深入的探究與概念理解。
經由以上的實驗觀察、討論與分析後,教師可將已形成金屬樹晶的正、負極反接,請同學由已學習的概念推測可能出現的實驗結果,經討論後,教師可進行實驗驗證同學們的推論,進而加強同學對氧化還原概念的瞭解,達到學生的學習目的。
.png) 結論
結論
在目前的電解硫酸銅溶液實驗中,實驗以燒杯(或U型管) 較大型裝置進行,實驗過程中學生只觀察到產物產生,而無產物產生的變化,只能記憶正負極的產物種類,對氧化還原概念的瞭解便較不深刻,更難有進一步對此現象的探索,且在實驗結束後,教師和學生對大量實驗廢液的處理更為一大問題。
微型電解裝置便可提供為較佳的實驗裝置,實驗採用微型電解裝置時,實驗中的電解質溶液(硫酸銅溶液) 為低濃度、低劑量,教師可藉此教導環保概念,也符合綠色化學精神,在實驗過程中,學生可觀察到銅金屬樹晶的生長過程與樣貌,進而對氧化還原的現象與概念更加深刻,也能欣賞到化學變化的美,以達到美感教學,若學生對此現象感到興趣,亦可使用微型電解裝置對電解實驗再進一步深入的探究。